三类医疗器械注册本服务是在国家药品监督管理下开展的境内Ⅲ类医疗器械(包含有源、无源、植入、无菌、义齿、IVD、软件)注册/延续/变更工作。
因篇幅有限,以下仅列出境内Ⅲ类医疗器械首次注册办理基本条件及流程,延续/变更事项及其他未尽事宜,请联系客服咨询。
证书有效期:5年(注册证延续注册需提前六个月办理)。
1、申报注册的产品已经列入最新版《医疗器械分类目录》,且管理类别为第三类;
2、申请人应当是依法进行登记的企业;
3、申请人建立与产品研制、生产有关的质量管理体系,并保持有效运行;
4、申请人申请注册,应当遵循医疗器械有效基本要求,保证研制过程规范,所有数据真实、完整和可溯源。
● 产品研发过程辅导
● 产品分类确认
● 检测单元确定
● 注册单元确认
● 产品技术要求预审核
● 产品样品送检文件准备辅导
● 产品送检风险管理文件编制辅导
● 产品送检及检验报告跟踪
● 生产厂房规划及平面图设计
● 生产设备及检验设备、设施清单确定
● 无菌或无尘厂房设施验证
● 灭菌工艺验证
● 包装工艺验证
● 特殊过程验证
● 产品UDI码申请,维护,实施辅导
● 注册资料申报辅导
● GMP人员培训
● 质量管理体系文件编制辅导
● 体系考核申报资料准备
● 同等考核申报资料递交
● 产品技术文档建立辅导
● UDI管理软件/批记录管理软件(医械ERP软件)实施,培训
● 体系考核现场预审
● 体系考核后不符合项整改辅导
● 注册资料发补辅导
● 非临床试验的临床评价辅导
● 临床试验CRO
● 临床试验备案
● 准确度验证辅导
● 企业委托设计
● 产品注册过程审评资料准备辅导
● 与主管机构联络及技术咨询
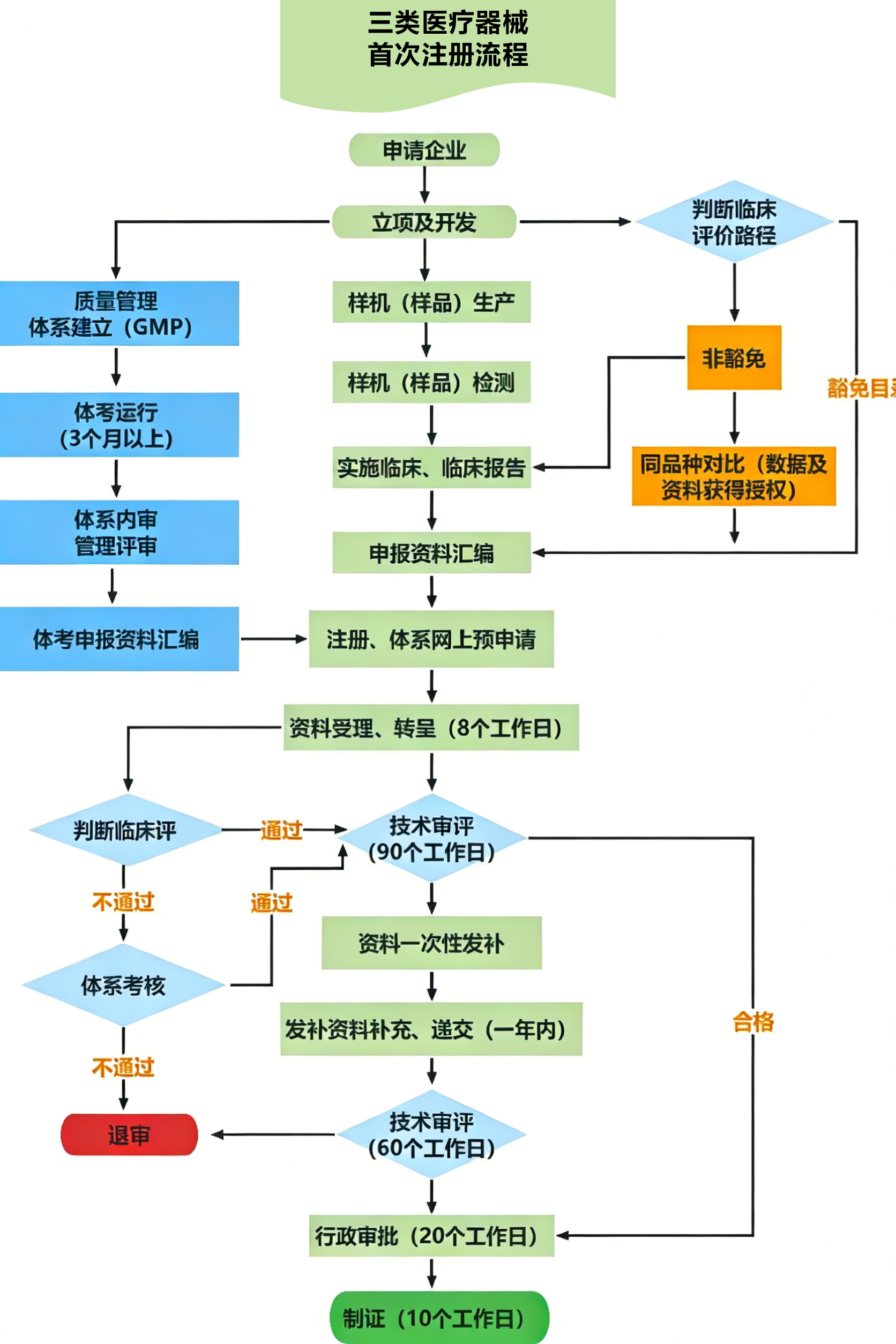
境内Ⅲ类医疗器械首次注册,预计约18个月(以国家官网行政时限为准!具体请联系客服咨询)。